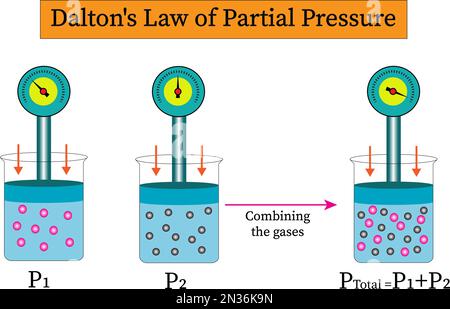
🧪 Daltons lov om partialtryk
Daltons lov beskriver, hvordan trykket i en gasblanding fordeler sig:
“Det samlede tryk i en gasblanding er lig med summen af de partialtryk, som hver enkelt gas ville udøve, hvis den var alene i samme volumen.”
🧮 Den matematiske formel
Hvis du har en gasblanding med flere komponenter, så gælder:
P_{\text{total}} = P_1 + P_2 + P_3 + \dots + P_n
Hvor:
- P_{\text{total}} = det samlede tryk
- P_1, P_2, \dots, P_n = partialtrykkene fra hver gas i blandingen
🌬️ Et praktisk eksempel
Forestil dig atmosfærisk luft:
- Den består hovedsageligt af nitrogen, oxygen, argon og lidt CO₂.
- Hver gas bidrager med sit eget tryk – og summen af disse er det atmosfæriske tryk (ca. 101,3 kPa ved havniveau).
🔍 Hvor bruges Daltons lov?
- I kemi og fysik til at beregne gasblandinger
- I medicin, fx ved iltbehandling og dykning
- I meteorologi og luftfart